Operacja zaćmy to jeden z najczęściej wykonywanych zabiegów chirurgicznych na świecie. W Polsce przeprowadzanych jest ponad 300 tysięcy zabiegów rocznie[1]. Trwa wyścig pomiędzy firmami medycznymi proponującymi coraz lepsze narzędzia i implanty chirurgiczne. Poszerza się spektrum materiałów i konstrukcji wykorzystywanych do produkcji soczewek wewnątrzgałkowych. Często uczymy się ich właściwości przez lata własnych doświadczeń i obserwacji. Materiały, z których produkowane są soczewki wewnątrzgałkowe wywołują specyficzną odpowiedź tkankową i tolerancję biologiczną określaną biokompatybilnością. W odniesieniu do IOL możemy mówić o biokompatybilności naczyniówkowej (reakcja komórkowa) oraz torebkowej (reakcja torebek soczewki)[2]. Poniżej przedstawiamy nasze doświadczenia z soczewką ASPIRA-aA.
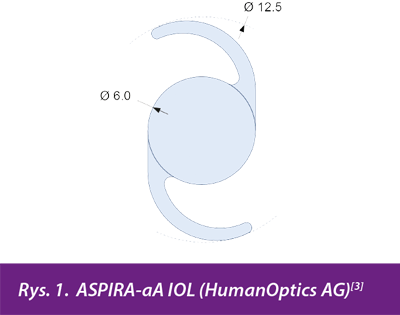
Soczewka ASPIRA-aA to jednoogniskowa, zwijalna, tylnokomorowa soczewka wewnątrzgałkowa (IOL) produkowana przez firmę HumanOptics (Erlangen, Niemcy). Jednoczęściowa konstrukcja z haptykami w kształcie litery „C” wykonana została z hydrofilnego akrylu (uwodnienie 26% w 35°), absorbującego promieniowanie UV. Przednia powierzchnia optyki ma konstrukcję asferyczną, zaś tylna ostra krawędź na obszarze 360° ma stanowić barierę dla migracji komórek nabłonkowych soczewki i zapobiegać zmętnieniu torebki tylnej (rys.1.[3]).
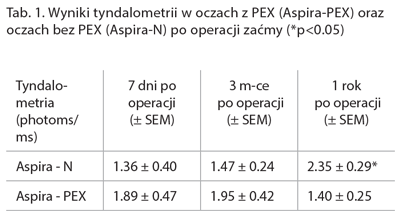
W Klinice Diagnostyki i Mikrochirurgii Jaskry w Lublinie w latach 2016-2018 ocenialiśmy biokompatybilność soczewki ASPIRA-aA (HumanOptics AG). Aby podwyższyć stopień trudności skupiliśmy się na porównaniu efektów w oczach z zespołem pseudoeksfoliacji (PEX) i grupie kontrolnej oczu z zaćmą bez innych patologii. Powszechnie wiadomo, że operacje zaćmy w oczach z PEX mogą być dużym wyzwaniem ze względu na częstsze powikłania śródoperacyjne (wąska źrenica, osłabienie obwódki rzęskowej, podwichnięcie lub zwichnięcie soczewki, uszkodzenie torebki) oraz pooperacyjne (przedłużający się odczyn zapalny, wzrost ciśnienia wewnątrzgałkowego, zmętnienie torebki, podwichnięcie lub zwichnięcie kompleksu z torebką – IOL). Nasze wyniki są następstwem przeprowadzenia 149 niepowikłanych operacji zaćmy metodą fakoemulsyfikacji z wewnątrztorebkową implantacją soczewki ASPIRA-aA (76 oczu z PEX oraz grupa kontrolna 73 oczy bez PEX). Wszystkie zabiegi wykonał jeden chirurg (T. Ż.). Badaliśmy biokompatybilność IOL w okresie 7 dni, 3 miesięcy i 1 roku po zabiegu. Reakcję komórkową szacowaliśmy na podstawie odczytu tyndalometru (Kowa FM-500) oraz subiektywnej obserwacji klarowności płynu w komorze przedniej. Wyniki badań pokazały, że reakcja zapalna po 7 dniach i 3 miesiącach po operacji była podobna w obu grupach, zaś po 1 roku po operacji istotnie mniejsza w oczach z PEX (tab.1.).
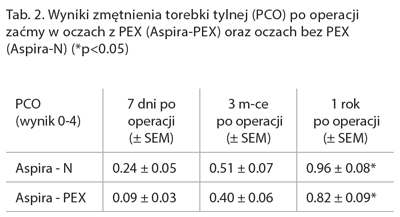
Reakcję torebkową analizowaliśmy na podstawie migracji oraz proliferacji komórek nabłonkowych soczewki (LEC = lens epithelial cells) na torebkę tylną (PCO = posterior capsule opacification) i przednią soczewki (ACO = anterior capsule opacification) oraz odrastanie LEC na przednią powierzchnię optyki IOL. PCO ocenialiśmy subiektywnie według 4-stopniowej skali, gdzie stopień 1 oznaczał minimalne, zaś stopień 4 ciężkie zmętnienie tylnej torebki soczewki[4]. Wyniki naszych obserwacji pokazały niskie PCO w obu grupach po 1 roku po operacji (0.82 ± 0.09 w oczach z PEX i 0.96 ± 0.08 w grupie kontrolnej) (tab. 2.).
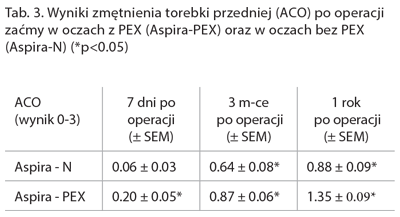
Intensywność zmętnienia torebki przedniej określaliśmy w skali 3-stopniowej, gdzie 1 oznaczał łagodne, a 3 ciężkie zmętnienie[5]. Rok po zabiegu stopień ACO był wyższy w oczach z PEX w porównaniu z grupą kontrolną (odpowiednio 1.35 ± 0.09 oraz 0.88 ± 0.09) (tab. 3.).
Powyższe wyniki badań potwierdzają dobrą biokompatybilność soczewki ASPIRA-aA (HumanOptics AG) wszczepianej w czasie operacji zaćmy. Nasze doświadczenia pokazują możliwość implantacji soczewki ASPIRA-aA z dużym powodzeniem zarówno w oczach z zaćmą niepowikłaną, jak i w oczach o podwyższonym ryzyku powikłań, do których niewątpliwie należą pacjenci z PEX.
Mamy nadzieję, że w dobie dostępności wielu materiałów, korzystanie z rozwiązań sprawdzonych w praktyce klinicznej pomoże w wyborze optymalnej IOL dla każdego pacjenta. ♦
Piśmiennictwo: [1] Kryteria kwalifikacyjne do operacji zaćmy. Rękas M. URL https://www.mp.pl/okulistyka/wytyczne/wytyczne-iartykuly/172546,kryteria-kwalifikacyjne-do-operacji-zacmy [2] Amon M. Biocompatibility of intraocular lenses. J Cataract Refract Surg. 2001;27(2):178-9 [3] https://www.humanoptics.com/en/physicians/intraocular-lenses/monofocal-1p-aspira/#d2 [4] Findl, O., et al., Comparison of 4 methods for quantifyingposteriorcapsuleopacification. J CataractRefractSurg, 2003. 29(1): p. 106-11 [5] Vock, L., et al., Effect of the hydrophilicity of acrylicintraocularlensmaterial and hapticangulation on anteriorcapsuleopacification. Br J Ophthalmol, 2007. 91(4): p. 476-80